お問い合わせ
有機チタン、有機ジルコニウム、その他有機金属化合物に関するご要望、製品に関するご質問や、
資料・サンプル請求をされる場合、また受託加工のご相談やお困りのこと等がございましたら
お気軽にお問い合わせください。
マツモトファインケミカル(株)営業部
TEL 047-393-6330
FAX 047-393-1063
カテゴリ
アーカイブ
2024年02月27日
テクニカルコラムNo.10では、ジルコニウムアルコキシドを用いたゾルゲル反応による耐アルカリ性膜形成の可能性についてご紹介いたします。
本記事に関するサンプルのご用命、ご質問等は以下のページからご相談ください。
チタンアルコキシドやジルコニウムアルコキシドを加水分解重縮合し、熱分解することによって、酸化チタンや酸化ジルコニウム膜が形成できます。これら酸化チタン、酸化ジルコニウム膜の耐酸性、耐アルカリ性は以下のような特性を有しています。
<表1. 酸化チタン、ジルコニウムの耐酸性、耐アルカリ性>
|
金属酸化物 |
酸、またはアルカリに対する溶解性 |
|
酸化チタン |
フッ化水素酸、熱濃硫酸、溶融アルカリ塩に溶解。 |
|
酸化ジルコニウム |
フッ化水素酸に溶解、水酸化ナトリウム硝酸、塩酸に微量に侵食される |
酸化ジルコニウムは、水酸化ナトリウムに微量に侵食されるものの、溶解することは無く、耐アルカリ性が高いことが予想されます。
ジルコニウムテトラn-ブトキシド(当社製品オルガチックスZA-65)とテトラエトキシシランを使用してZrO2-SiO2膜を形成した際の耐アルカリ性について以下文献で紹介されています。
峠 昇、松田 厚範、南 勉(1987)ゾル・ゲル法によるZrO2およびZrO2-SiO2コーティング薄膜の作製、日本化学会誌 1987 No.11
本文献におけるZrO2-SiO2膜の形成工程は以下の通りです。
① ジルコニウムテトラn-ブトキシドをエタノール溶液に溶解した後、空気中で攪拌することで、空気中の水分と徐々に反応させてオリゴマー化
② テトラエトキシシランを混合
③ グローブボックス内でディップ法によってスライドガラスに塗布し、600℃の環境下で10分間焼成
尚、ZrO2とSiO2のモル比について、(100-x)ZrO2・xSiO2とした際、x=50mol%以上になるとガラス基材への濡れが悪く製膜が困難との記述がありました。
文献では、この原因としてテトラエトキシシランとジルコニウムテトラn-ブトキシドの加水分解速度に着目し、今回の条件ではテトラエトキシシランの加水分解があまり進まなかったために濡れ性が悪くなったと記載されていました。
本記述に関し、当社で検証実験を行いました。
検証実験の結果、テトラエトキシシランに対して5wt%程度のジルコニウムテトラn-ブトキシドを添加したところ白色のゲル物質が生成しました。
一方、ジルコニウムテトラn-ブトキシドに対して5wt%のテトラエトキシシランを添加してもゲル化せず、均一溶液となったことが確認されました。
本挙動は、テトラエトキシシランがメインの組成の場合、エトキシ基の酸素原子がジルコニウム原子に配位することによってポリマー化して白色ゲルを形成したのではないかと推測します。
逆の量比の場合は、上述のポリマーが配位構造を形成していないジルコニウムテトラn-ブトキシドに溶解して均一溶液として存在しているのではないかと推測します。
当社の実験結果からは、SiO2源であるテトラエトキシシランをメインとした透明な塗布液を作製し、均一な膜を得ることは無溶剤では難しいと考えます。
均一膜をガラス基材に形成するのであれば、n-ブタノール等の希釈溶剤を併用することが必要と考えます。
2-1.で示した工程で得られた膜の耐アルカリ性の測定結果を図1に示します。
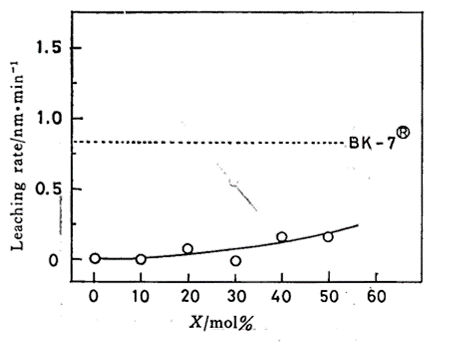
<図1.ZrO2-SiO2膜の耐アルカリ性>
図1は、50℃の3mol/LNaOH水溶液にZrO2-SiO2膜を形成したスライドガラス(BK-7®)を浸漬した後、溶出した膜厚を測定して溶出速度の差を確認した結果です。
横軸は(100-x)ZrO2・xSiO2で表記されるモル比、縦軸は浸出率です。
膜の組成においてZrO2のモル比が低下することで、浸出率、すなわちガラスがどの程度溶解するかを示した線図となります。
また、図中、破線で示したのは表層にZrO2-SiO2膜が無い場合の浸出率を示しています。
スライドガラスに比べて、x=30mol%においてほとんど溶出による膜厚変化はなく、40mol%以上でわずかに溶出していることが分かります。
このように、膜中にZrO2が存在することで、耐アルカリ性が発現しています。
上述の文献では、ジルコニウムテトラn-ブトキシドをエタノールに溶解した後、空気中の水を使用して徐々に加水分解重縮合反応を進めていました。
加水分解重縮合反応を行う理由は、
①モノマーよりもZr-O-Zr結合をもつオリゴマー体の方が、製膜性が良好である
②加水分解重縮合反応速度が遅いテトラエトキシシランに近づけるため
の2点があると推測します。
当社での実験では、ジルコニウムテトラn-ブトキシド等のジルコニウムアルコキシドを溶剤で数%に希釈しても、直接水を添加すると、(水)酸化チタンが生成し、沈殿した経験があります。
このように、加水分解重縮合反応は非常に速く進行するため、空気中の水分で徐々に反応を進めたと考えられます。
一方、空気中の水分による急激な(水)酸化ジルコニウムの生成を防ぐ目的で、グローブボックス内で塗布を行っていました。
工業的な製膜を考えた場合、製膜時の空気中の湿度によって形成される膜が異なる可能性があります。このことは、品質確保の面で難しく、また、グローブボックスのような密閉空間で工業的に生産することは難しいと考えます。
工業的な製膜を考えると、加水分解重縮合反応性が低く、水に対して安定な化合物が好ましいと考えます。
このような化合物としては、テクニカルコラムでは何度か述べていますが、やはりキレート化合物を用いることが良策といえます。
基材がガラス、金属、セラミックス等の耐熱性に優れた基材の場合、有機ジルコニウム化合物を熱分解させ酸化ジルコニウムにできる300℃以上の加熱が可能であることから、図2で示すアセチルアセトンやアセト酢酸エチルのようなβジケトン、βケトエステル等のキレート化合物を使用することが適当であると考えます。
<図2. ジルコニウムキレート化合物>
その他の方法としては、上述の文献のようにジルコニウムアルコキシドのオリゴマー体を使用することが考えられますが、加水分解重縮合反応速度の観点から合成が非常に困難なため、当社においても条件最適化に向け現在研究中です。
今回は、ジルコニウムアルコキシドを使用したゾルゲル法による耐アルカリ性膜の形成について紹介しました。
文献では、耐アルカリ性を示すZrO2-SiO2膜を作製するためにジルコニウムアルコキシドを使用していましたが、工業的な観点においては、キレート化合物を選択した方が良いと考えます。
本内容にご興味がございましたら、お気軽にお問い合わせください。
関連するテクニカルコラム
テクニカルコラムNo.9 有機チタン、ジルコニウム化合物のゾルゲル反応を用いた部分加水分解~オリゴマー化合物の合成~
有機チタン、有機ジルコニウム、その他有機金属化合物に関するご要望、製品に関するご質問や、
資料・サンプル請求をされる場合、また受託加工のご相談やお困りのこと等がございましたら
お気軽にお問い合わせください。
マツモトファインケミカル(株)営業部
TEL 047-393-6330
FAX 047-393-1063